저작자: 강기봉 freekgb@gmail.com
□ ㈜에스케이바이오사이언스 개발 코로나19 백신 ‘GBP510’ 3상 임상시험 승인
(인용: 국내 개발 코로나19 백신 3상 임상시험 승인(식품의약품안전처 보도자료, 2021.8.10.))
식품의약품안전처(이하 식약처)에 따르면, (주)에스케이바이오사이언스(전 에스케이케미칼, 이하 SK바이오사이언스)는 국내 개발 코로나19 백신 ‘GBP510’에 대해 국내 최초로 국산 코로나19 백신의 3상 임상시험 계획을 8월 10일(화) 승인했습니다. 이 3상 임상시험은 기 허가된 백신과의 비교로 효과를 입증하는 비교임상 방식으로는 세계에서 2번째라고 합니다.
* 1번째 : 2021.4. 프랑스 발네바社가 개발한 코로나19 백신이 아스트라제네카 백신을 대조군으로 하는 비교임상(3상)을 승인받아 영국에서 임상을 시작
* 면역원성 비교임상 : 시험백신의 효능을 안전성과 유효성이 입증된 기허가된 백신(대조군)의 면역원성과 비교하여 대조백신보다 우월하거나 열등하지 않음을 보여주는 임상
- 비열등성 시험(Non-inferiority Trial) : 시험군이 미리 정한 비열등성 마진의 범위 내에서 대조군보다 나쁘지 않음을 보여주는 임상시험 설계
- 우월성 시험(Superiority trial) : 시험군이 1차 평가변수를 근거로 대조군보다 우월함을 증명하는 것을 일차적인 목적으로 하는 임상시험 설계
| 임상시험 단계 - (임상 1상) 최초로 사람에게 투여하여 안전성, 약동학 등을 평가 - (임상 2상) 1상 종료 후, 대상 환자들에게 투여하여 치료효과를 탐색 - (임상 3상) 2상 종료 후, 많은 환자들에게 투여하여 안전성 및 치료효과를 확증 ※ ‘1상과 2상’(1/2상) 또는 ‘2상과 3상’(2/3상)을 동시 승인하는 경우도 있음 |
□ 코로나19 백신 ‘GBP510’ 3상 임상시험 현황
- 3상 개요 : 만 18세 이상의 성인을 대상으로 면역증강제 AS03(Adjuvant System 03)을 이용한 SARS-CoV-2 재조합 단백질 나노입자 백신(GBP510)의 면역원성 및 안전성을 평가하기 위한 다기관, 평행 비교, 관찰자 눈가림, 활성 대조, 무작위배정 제3상 임상시험
- 임상시험 기간 : 2021년 8월 ~ 2022년 12월
□ ‘GBP510’의 개발 원리
식약처에 따르면, SK바이오사이언스 개발 백신은 유전자 재조합 기술을 이용해 만든 코로나19 바이러스의 표면항원 단백질을 주입해 면역반응을 유도하는 `재조합 백신’이라고 합니다. 표면항원 단백질을 투여하면 체내에서 면역세포를 자극해 중화항체 생성을 유도하며, 인체에 코로나19 바이러스가 침입했을 때 바이러스를 중화해 제거하게 되는 원리로, 현재 독감백신, B형 간염, 자궁경부암 백신 등 백신 생산에 많이 사용되고 있는 제조 플랫폼이라고 합니다(인용: 국내 개발 코로나19 백신 3상 임상시험 승인(식품의약품안전처 보도자료, 2021.8.10.)).
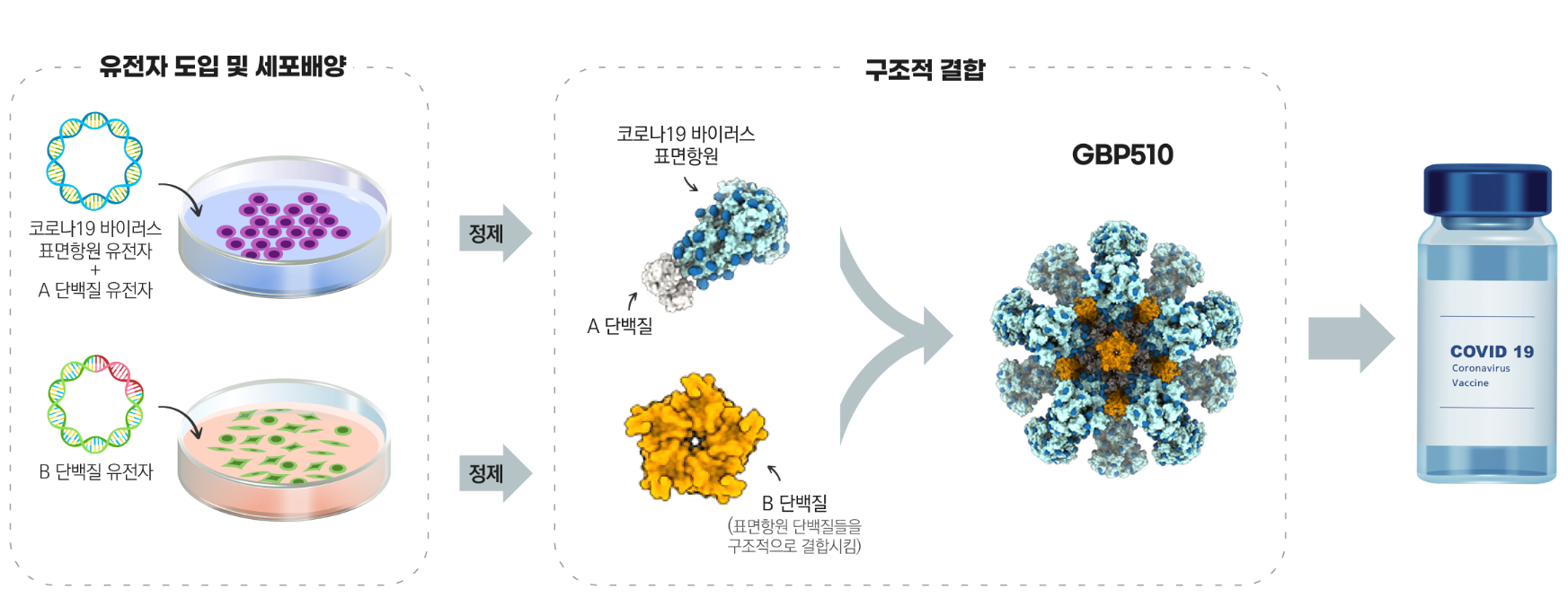
※ 위 표면하원 단백질은 S 단백질(S-protein, 표면돌기 단백질)로 생각됩니다. 논문자료에 따르면, S 단백질은 바이러스 표면에 노출되어 숙주의 면역시스템에 직접적으로 인식되는 부분이며, 숙주세포의 ACE2 수용체에 결합 후 숙주세포 안으로 들어가 병원성을 유발하는 데 필수적으로 작용합니다. 이러한 이유로 SARS-CoV 및 MERS-CoV에 대한 백신개발에서 S 단백질이 사용되었다고 합니다(So-Hee Hong, et al, Lessons Learned from SARS-CoV and MERS-CoV: Preparation for SARS-CoV-2 induced COVID-19, J Bacteriol Virol. Vol 50. No 2. June 2020, p.84, https://doi.org/10.4167/jbv.2020.50.2.076).
※ 인용 정보 : 국내 개발 코로나19 백신 3상 임상시험 승인(식품의약품안전처 보도자료, 2021.8.10.), https://www.mfds.go.kr/brd/m_99/view.do?seq=45642&srchFr=&srchTo=&srchWord=&srchTp=0&itm_seq_1=0&itm_seq_2=0&multi_itm_seq=0&company_cd=&company_nm=&Data_stts_gubun=C1009&page=1
□ 관련 기사 : SK바이오사이언스-GSK, 코로나19 백신 개발 협력 (SK바이오사이언스 보도자료, 2021.02.05)
보도자료에 따르면, SK바이오사이언스는 BMGF(빌&멜린다게이츠재단), CEPI(전염병대비혁신연합)의 지원을 받고 있는 코로나19 백신 후보물질 ‘GBP510’에 글로벌 제약사 GSK(GlaxoSmithKline)의 면역증강제(Adjuvant) ‘AS03’를 병용 투여하는 임상1/2상을 시작했다고 2021년 2월 4일 밝혔습니다(위에 기술한 바와 같이 현재는 3상 임상시험 중입니다).
면역증강제는 일부 백신 제형에 추가 투여함으로써 면역 반응을 유도하는 백신 항원물질의 체내 이동을 촉진하고 항원 자극 시간을 늘려 단독 투여 시 보다 백신의 효과를 향상시키는 보조제라고 합니다. SK바이오사이언스는 자체적으로 진행한 GBP510 동물시험에서 AS03 병용 투여 시 보다 높게 유도된 중화항체와 체액성 및 세포성 면역반응을 유도하는 T세포 활성의 증가를 확인, GSK와 협력을 결정했다고 합니다.
※ AS03 정보 : https://en.wikipedia.org/wiki/AS03
※ 인용 정보 : SK바이오사이언스-GSK, 코로나19 백신 개발 협력 (SK바이오사이언스 보도자료, 2021.02.05), https://www.skbioscience.co.kr/kr/news/news_01_01?mode=view&id=40
□ SK바이오사이언스의 특허출원
현재 SK바이오사이언스의 GBP510에 대해 직접적으로 공개된 특허출원 자료는 찾기 어렵습니다. 그렇지만 SK바이오사이언스는 MERS-CoV 외에 RSV, 폐렴구균, 인플루엔자 등의 홉흡기 관련 백신에 대한 특허출원을 한 상태입니다. 아래 정보는 특허정보넷 키프리스(http://www.kipris.or.kr/)에서 인용하였습니다.
- RSV에 관한 특허출원
- RSV의 F 단백질-항체 복합체 및 이를 포함하는 조성물
Antibody complexed F protein of RSV and composition comprising the same
출원번호/일자 1020190062794 (2019.05.28)
공개번호/일자 1020200136774 (2020.12.08)
- 재조합 RSV 생백신주 및 이의 제조 방법
Recombinant RSV live vaccine strain and the preparing method thereof
출원번호/일자 1020190127265 (2019.10.14)
공개번호/일자 1020200041821 (2020.04.22)
- 재조합 호흡기 세포융합 바이러스 F 단백질 및 이를 포함하는 백신 조성물
Recombinant RSV F protein and vaccine composition comprising thereof
출원번호/일자 1020180133084 (2018.11.01)
공개번호/일자 1020200050264 (2020.05.11)
- MERS-CoV에 관한 특허출원 : ‘GBP510’의 기초가 되었을 것으로 추정됩니다.
- 중동호흡기증후군 코로나바이러스 S 단백질 면역원 조성물 및 이의 제작 방법
Immunogenic Middle East Respiratory Syndrome Coronavirus (MERS-CoV) S protein composition and producing method thereof
출원번호/일자 1020170156624 (2017.11.22)
공개번호/일자 1020180058206 (2018.05.31)
요약 : 본 발명은 서열번호 2, 4, 6 및 8로 이루어진 군에서 선택된, 어느 하나 이상의 폴리펩타이드를 포함하는 MERS-CoV S 면역원성 조성물 및 이의 제조방법을 제공한다. 본 발명의 제조방법을 통해 제조된 면역원성 조성물은 높은 수율을 기대할 수 있으며, 우수한 MERS-CoV 예방을 위한 조성물을 제공할 수 있다.
□ 향후 전망
(주)셀트리온의 렉키로나주 코로나19 치료제는 3상 임상시험 초기에 사용 허가를 신청하여 허가를 받은 전례가 있습니다(참고 https://cblaw.net/198?category=496782). 치료제와 백신이라는 차이가 있지만, 향후에 코로나19 상황에 따라 (임상시험에서 특별한 문제가 발생하지 않는다면) 3상중에 사용 허가를 받게 될 수도 있을 것으로 보입니다.
'SW와 과학기술 > 바이오' 카테고리의 다른 글
| (주)제넨셀 ES16001 코로나19 치료제 2/3상 임상시험 승인 및 시행 (0) | 2021.10.27 |
|---|---|
| 국내개발 코로나19 백신 및 치료제 3상 임상시험 (0) | 2021.10.14 |
| (주)셀트리온 코로나19 치료제 '렉키로나주' 변경허가 (0) | 2021.09.18 |
| (주)제넨셀 코로나19 치료제 특허발명 및 개발 현황 (0) | 2021.08.30 |
| (주)셀트리온의 렉키로나주 코로나19 치료제 특허 및 임상 현황 (0) | 2021.08.20 |


